Pierwiastki chemiczne dzielą się na metale i niemetale. Metale to substancje, które przewodzą prąd, mogą tworzyć arkusze lub druty i mają połysk. Niemetale to wszystkie substancje, które nie przewodzą prądu, są kruche w obsłudze lub są gazami.
Główną cechą odróżniającą metale od niemetali jest zdolność do przewodzenia prądu.
Istnieją pierwiastki, które wyglądają jak metale, ale reagują jak niemetale. Pierwiastki te znane są jako metaloidy i obejmują bor, krzem, german, arsen, antymon, tellur i polon.
| Metale | Niemetale | |
|---|---|---|
| Definicja | Są to pierwiastki, które mają skłonność do tracenia elektronów i przewodzenia prądu. | Są to pierwiastki o tendencji do zyskiwania elektronów i są słabymi przewodnikami prądu. |
| Cechy |
|
|
| Przykłady |
|
|
Spośród 118 pierwiastków w układzie okresowym metale stanowią 80%. Oto pierwiastki układu okresowego i odpowiadająca im klasyfikacja jako metale, niemetale i metaloidy:
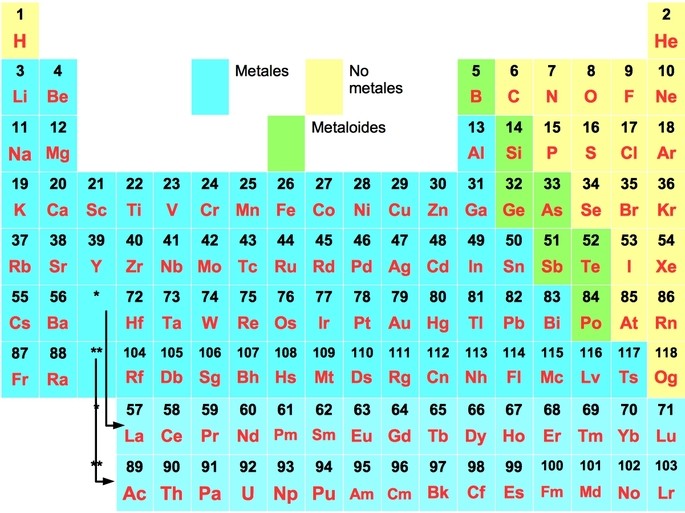
Co to są metale?
Pierwiastki metaliczne to takie, które mają skłonność do oddawania elektronów i mogą przewodzić prąd elektryczny. Mają też charakterystyczny połysk, są kowalne i ciągliwe.
Znajdują się one po lewej stronie układu okresowego, przy czym pierwiastki najbardziej wysunięte na lewo mają charakter najbardziej metaliczny.
Metale można podzielić na:
- Metale alkaliczne to pierwiastki: lit, sód, potas, rubid, cez i frank.
- Metale ziem alkalicznych to pierwiastki: beryl, magnez, wapń, stront, bar i rad.
- Metale przejściowe to te, które występują w środkowym bloku układu okresowego, a należą do nich m.in. miedź, złoto, srebro, platyna.
Właściwości metali
- Przewodzić prąd : umożliwiają ruch elektronów przez materiał.
- Ich elektrony walencyjne poruszają się swobodnie Elektrony w najbardziej zewnętrznej warstwie metali mogą się swobodnie poruszać.
- Są podatne na utratę elektronów kiedy metale reagują, zwykle tracą elektrony.
- Są one reaktywne Reaktywność chemiczna metali rośnie w dół przez grupę, ale maleje w okresie.
- Są one połączone wiązaniami metalicznymi Metale tworzą ze sobą wiązania metaliczne - morze elektronów, które "spacerują" między jądrami atomów.
- Są stałe w temperaturze pokojowej Większość metali to ciała stałe, z wyjątkiem rtęci Hg, galu i cezu, które w temperaturze pokojowej są cieczą.
Przykłady metali
Aluminium
Jest to najobficiej występujący w skorupie ziemskiej metal o srebrzystobiałym, jasnym połysku i liczbie atomowej 13. Jest ciałem stałym, które topi się w temperaturze 660°C. Aluminium wydobywa się z boksytu, który jest formą uwodnionego tlenku glinu.
Jest szeroko stosowany w naczyniach kuchennych i zastosowaniach przemysłowych ze względu na wysoką odporność na korozję.

Puszka po napoju bezalkoholowym wykonana jest z aluminium.
Bar
Jest to metal o liczbie atomowej 56, należący do metali ziem alkalicznych.Jest to ciało stałe, które topi się w temperaturze 727 ºC, odkryte w 1808 roku przez Humphreya Davy'ego.Otrzymuje się go z barytu, soli siarczanu baru.
Bar w czystej postaci ma srebrzysty wygląd jak ołów.
Beryl
Jest czwartym pierwiastkiem w układzie okresowym, należącym do metali ziem alkalicznych. Jest ciałem stałym, które topi się w temperaturze 1287 ºC i występuje w składzie szmaragdów i akwamarynów.

W składzie akwamarynu znajduje się beryl.
Bizmut
Jest to kruchy, krystaliczny, biały metal o liczbie atomowej 83, długo mylony z cyną lub ołowiem. Jest najbardziej diamagnetyczny z metali i ma najmniejszą zdolność do przenoszenia ciepła. Bizmut jest produkowany w stopach do powlekania przedmiotów, które mogą być uszkodzone w wysokich temperaturach, takich jak sprzęt do wykrywania ognia lub gaśnice.
Wapń
Jest piątym najobficiej występującym pierwiastkiem metalicznym w skorupie ziemskiej. Ma srebrzysty kolor, jest twardym ciałem stałym, o liczbie atomowej 20. Należy do metali ziem alkalicznych i jest składnikiem ważnych struktur biologicznych, takich jak kości, zęby i muszle.
Cez
Jest to najbardziej elektroujemny i zasadowy metal.W temperaturze pokojowej występuje w stanie ciekłym, obok galu i rtęci.Cez wybucha w kontakcie z wodą i ma duże powinowactwo do tlenu.Jest stosowany w zegarach atomowych.
Chrom
Jest to jeden z metali przejściowych, o liczbie atomowej 24, ciało stałe, które topi się w temperaturze 2671 ºC. Chrom jest używany do hartowania stali, aby nadać jej twardą, błyszczącą powierzchnię, aby zapobiec korozji oraz w produkcji szkła, aby nadać mu zielony kolor.
Miedź
Jest jednym z najważniejszych metali dla ludzkości, która używa go od ponad 5000 lat. Wyróżnia się czerwonawym, metalicznym połyskiem, a ponadto jest kowalny i plastyczny, co pozwala na stosowanie go w budowie biżuterii, naczyń kuchennych i urządzeń elektrycznych.

Miedź jest szeroko stosowana w przemyśle elektrycznym ze względu na jej zdolność do przewodzenia prądu.
Iron
Jest to najbardziej rozpowszechniony metal na Ziemi, ponieważ stanowi dużą część jądra naszej planety. Jego liczba atomowa wynosi 26, jest twardym, kruchym ciałem stałym, które topi się w temperaturze 1538 ºC. Żelazo jest częścią systemów transportu tlenu w organizmach żywych. W czystym stanie żelazo jest bardzo reaktywne i szybko ulega korozji w wilgotnym środowisku.
Złoto
Jest to najbardziej plastyczny i ciągliwy metal, o wielkim pięknie w czystym stanie.Jego liczba atomowa wynosi 79 i należy do metali przejściowych.Jest dobrym przewodnikiem elektryczności i ciepła oraz odporny na korozję.Był używany jako waluta i jest obecnie standardem w systemie monetarnym wielu krajów.

Łatwość obróbki złota pozwala na manipulowanie nim w celu tworzenia biżuterii i monet.
Co to są niemetale?
Pierwiastki niemetaliczne to wszystkie te pierwiastki, które nie pasują do charakterystyki metali. Do niemetali zalicza się halogeny, gazy szlachetne, wodór, węgiel, azot, fosfor, tlen, siarkę i selen.
Znajdują się one po prawej stronie układu okresowego, oddzielone od metali metaloidami.
Właściwości niemetali
- Nie przewodzą prądu elementy niemetaliczne są słabymi przewodnikami prądu.
- Ich elektrony walencyjne są ograniczone elektrony niemetali są bardziej ograniczone w swoim ruchu.
- Są skłonne do zdobywania elektronów : atomy pierwiastków niemetalicznych mają tendencję do przyjmowania elektronów od innych pierwiastków podczas reakcji.
- Mają reaktywność Reaktywność chemiczna niemetali maleje w grupie, ale rośnie w okresie.
- tworzą wiązania kowalencyjne z innymi niemetalami pierwiastki niemetaliczne mają tendencję do dzielenia się swoimi elektronami w powłoce walencyjnej z innymi niemetalami, tworząc wiązania kowalencyjne.
Może zainteresują Cię również Rodzaje wiązań chemicznych
Przykłady niemetali
Bromo
Jest to jedyny pierwiastek niemetaliczny występujący w temperaturze pokojowej jako czerwonobrązowa ciecz. Jego liczba atomowa wynosi 35 i należy do grupy halogenów. Wykorzystywany jest do produkcji środków ogniotrwałych, środków do oczyszczania wody, barwników, leków i środków dezynfekujących.
Węgiel
Jest to pierwiastek niemetaliczny o największej zdolności łączenia się z innymi pierwiastkami, klucz do budowy cząsteczek biologicznych. W przyrodzie występuje w stanie wolnym jako diament i grafit. W atmosferze występuje w połączeniu z tlenem jako dwutlenek węgla.

Grafit to naturalna forma węgla, która służy do pisania i rysowania.
Może zainteresują Cię również Przykłady związków organicznych i nieorganicznych.
Chlor
Jest to zielonkawo-żółty gaz, o liczbie atomowej 17, należący do grupy halogenów. Występuje w przyrodzie w połączeniu z innymi pierwiastkami, np. z solą kuchenną NaCl. Związki chloru są szeroko stosowane na całym świecie, m.in. jako środki dezynfekcyjne, wybielacze, do oczyszczania wody.
Fluor
Jest najbardziej elektronegatywnym i reaktywnym pierwiastkiem, należącym do grupy halogenów, o liczbie atomowej 9. W stanie czystym jest bladożółtym żrącym gazem.
Helio
Jest drugim pierwiastkiem układu okresowego i pierwszym pierwiastkiem grupy gazów szlachetnych.Jego nazwa pochodzi od greckiego helios co oznacza "słońce", gdzie został po raz pierwszy zidentyfikowany w 1868 r. Wraz z wodorem jest najobficiej występującym pierwiastkiem w całym wszechświecie.
Może Cię również zainteresować zobacz:
- Protony, neutrony i elektrony
- Przewodniki, izolatory i półprzewodniki.
Referencje
Lide, D. R. (editor) (2005) CRC Handbook of chemistry and physics, CRC Press, Boca Raton, Florida.
Vernon, R.E. (2013), Which elements are metalloids - Journal of Chemical Education 90:1703.